香港科技大学(科大)联同香港大学(港大)与法国居礼研究所共同发现了人体MCM2至MCM7蛋白复合体(Minichromosome Maintenance 2-7,微小染色体维持蛋白2-7)调控DNA 复制起始(Replication Initiation)的新机制。 此发现可被应用于研发新型、高效及更具针对性的抗癌药物。这项研究成果现已刊登在国际顶尖科学期刊《细胞》杂誌上(按此浏览期刊文章)。
我们的生命由单个受精卵细胞形成时开始。在母体子宫内,受精卵通过细胞分裂而发育成多细胞个体。在每次分裂中,编码遗传信息的基因组DNA都会被准确复制。每个细胞携带的DNA总长度约为两米,其通过摺叠、整合成为23对染色体。在人的一生中(约70年),人体将合成接近一光年长度的DNA(10^16米)。在复制的过程中,首先须利用解旋酶将双链DNA分解成两条单链DNA,其后DNA聚合酶以此为模板,合成两条新的互补配对的双螺旋DNA。若调控过程中出现一丝紊乱,都可能导致严重后果,例如肿瘤或遗传疾病等。
「破解DNA复制的机制是认识生命奥秘的关键。」领导这项研究的港大生物科学学院助理教授翟元樑博士说。「而解析复制机器蛋白质结构是了解其分子功能最核心的步骤,因为只有亲眼看到,才能相信。」
自1953年詹姆斯‧华生和弗朗西斯‧克里克解析DNA双螺旋结构以来,DNA双链最初是如何被解旋并打开,一直是个未解之谜。1983年,本研究的合作伙伴、康奈尔大学的戴杨碧瓘教授在酿酒酵母中发现了真核生物的DNA解旋酶基因—— MCM 。 随后的研究发现,六个MCM基因编码、由MCM2至MCM7蛋白形成的一个六亚基环状复合体,构成DNA解旋机器的活性中心。在细胞体内,DNA复制的起始须要由MCM2-7首先组装到染色体上成千上万个复制原点,并形成环绕双螺旋DNA的双六聚体(double hexamer, DH)。其后,一部分的MCM 2-7 DH被激活成为高效的DNA复制解旋酶。一直以来,研究人员认为MCM2-7 DH具有直接解旋和打开双链DNA的能力,但其作用机制尚不清楚。
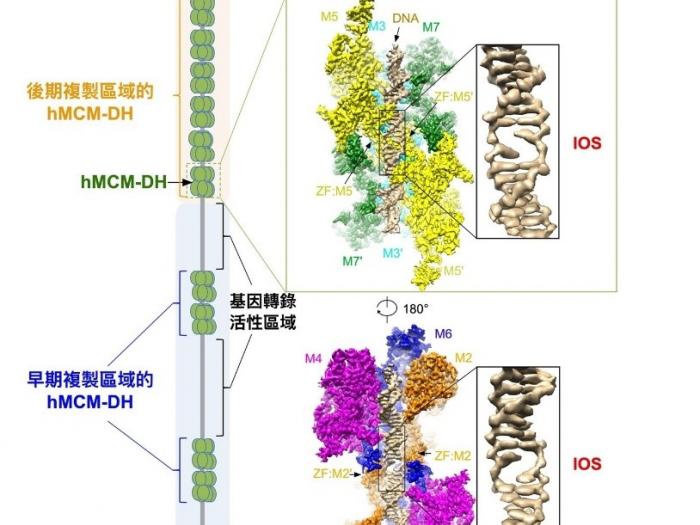
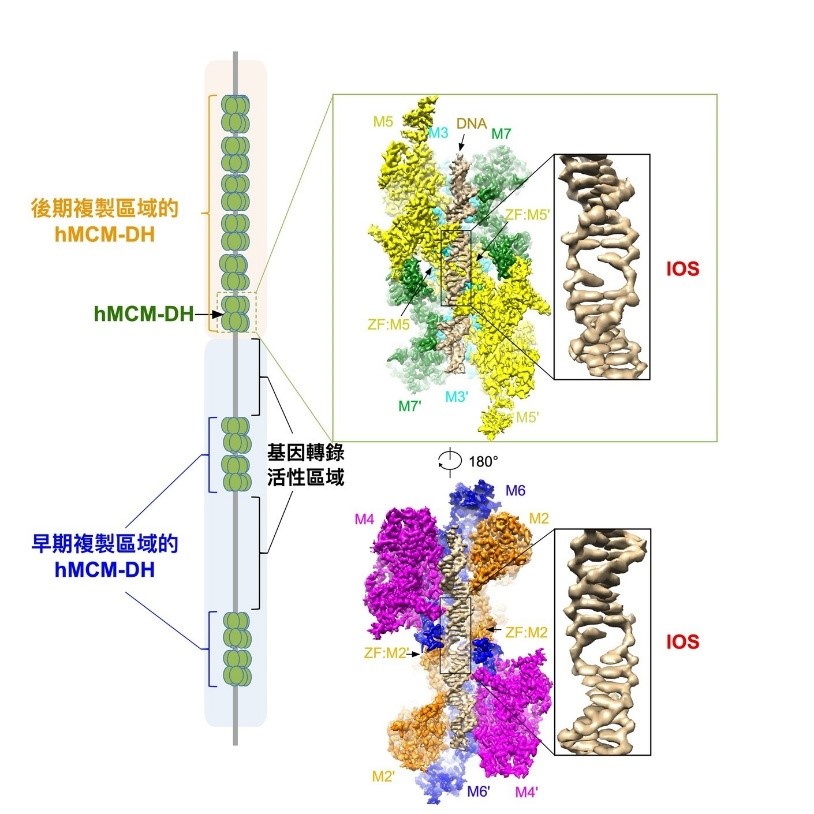
为了解开这个疑团,团队使用当今最前沿的冷冻电镜技术,研究以肉眼无法观测的MCM2-7 DH原子分辨率的高分辨结构,从而了解该蛋白复合体的工作原理。在2015年,团队首次解析了从酿酒酵母提纯的MCM2-7 DH的冷冻电镜结构,相关研究成果已在国际知名期刊《自然》上发表 (按此浏览期刊文章)。可惜的是,在该次研究中获得的结构,其复制原点 DNA非常不稳定,因而无法提供其双螺旋状态的信息。幸而,该团队近日终于成功纯化出人源MCM2-7 DH复合物,并能解析其原子分辨率达2.59埃的高精度结构。该结构清晰地展示MCM2-7 DH聚合体直接降低DNA双链的稳定性,并将位于两个六聚体结合处的双链DNA解旋,形成一个初始开口,从而将MCM2-7 DH牢固结合在初始打开的原点DNA上,遍佈整个基因组上没有活跃的「信使RNA(mRNA)」转录的区域。该研究发现,如果DNA初始开口的结构被破坏或干扰,所有的 MCM2-7 DH将无法稳定地在DNA上结合,从而完全抑制DNA复制的起始。
「原子分辨率的冷冻电镜结构使我们可以直接观测到DNA的解离,这对于理解DNA复制的分子机制至关重要。」科大生命科学部助理教授党尚宇博士说。「这项研究同时也说明了合作的重要性。为了解答最根本的生物学问题,往往需要来自具备不同专长的研究团队共同努力。」
一直以来,DNA复制是多个癌症治疗药物的作用靶点。然而,由于现有药物往往具有较大毒性,而正常细胞和癌症细胞均会在增殖过程中进行DNA复制,导致治疗过程中,药物无差别地杀死癌症细胞和正常细胞。
目前,如何提高化疗药物作用的针对性,一直是研发抗癌化合物的重要考量。在现阶段,一个理想方案是通过抑制DNA复制起始,使正常细胞滞留在G1期(细胞分裂的一个阶段)或者在G0期(细胞停止分裂的阶段)静止;在此情况下,癌症细胞则因其调控机制的紊乱,无法像正常细胞一样被保护在相应的细胞週期,从而进入诱导细胞凋亡。因此,阻断细胞复制起始,有望成为一种全新的、有效的、高度特异针对癌症细胞的抗癌疗法。该研究揭示的人源复制前始复合物的蛋白结构和工作机制,为以MCM2-7复合体为靶点的无毒抗癌药物开发提供了设计思路和重要的结构基础。
研究团队
研究团队由港大生物科学学院的翟元樑博士领导,成员包括科大生命科学部的党尚宇博士、科大高等研究院的戴杨碧瓘教授、法国居礼研究所的陈春龙博士、香港理工大学(理大)应用生物学和化学技术系的赵倩博士。
论文其他作者包括:港大生物科学学院的李健先生、范欣雨女士、许恩捷女士、李淑君博士、林玮熙博士; 科大生命科学部的董江清博士、余大启博士;法国居礼研究所的王纬韬博士、Nathan Alary先生;科大冷冻电镜中心的张盈怡博士;理大应用生物学和化学技术系的杨阳先生。
鸣谢
这项研究中所有冷冻电镜数据均在香港科技大学生物冷冻电镜中心收集,该中心得到罗桂祥基金会的慷慨资助。两位共同第一作者,董江清博士和余大启博士获得罗桂祥奖学金支持。
图片下载及説明:https://www.scifac.hku.hk/press
媒体查询
香港大学理学院
杜之桦(电话:3917-4948; 电邮:caseyto@hku.hk)
陈诗迪(电话:3917-5286; 电邮:cindycst@hku.hk)
香港科技大学公共事务处
冯惠仪(电话:2358-6307;电邮:fannyfung@ust.hk)