2015年7月29日,香港科技大學戴碧瓘(Bik-Kwoon Tye)教授和清華大學的高寧教授的研究團隊共同在《自然》(Nature)雜誌以長文形式發表題為《真核生物DNA複製解旋酶MCM複合物的3.8 Å分辨率結構》(Structure of the Eukaryotic MCM Complex at 3.8 Å)的研究論文,首次揭示DNA複製解旋酶MCM2-7複合體的高分辨率(3.8 Å)冷凍電鏡結構。這研究成果為人類認識及了解自身DNA複製起始過程的機制揭開新一頁。
DNA是所有生物遺傳信息的載體。六十多年前,當諾貝爾獎獲得者Watson和Crick發現DNA雙螺旋結構的時候,他們就預測到,在DNA複製過程中,需要解開緊密結合的雙鏈DNA,以便互補的DNA雙鏈各自作為範本進行複製。從那時起,關於DNA雙螺旋解鏈機理的研究,一直是生物學領域的研究熱點。
早在1983年,戴碧瓘教授在康奈爾大學的實驗室,率先發現MCM2-7基因,並證明這些基因在真核生物DNA複製過程發揮非常重要的作用。隨後的科學研究進一步發現,MCM2-7複合物負責在DNA複製起始和延伸階段作為雙鏈DNA的解螺旋酶。在真核生物細胞,整個DNA複製的過程都受到嚴格調控,以確保DNA遺傳信息能被準確複製。複製過程中的異常或缺陷會導致基因組不穩定,包括DNA雙鏈的斷裂、基因突變、染色體缺失,這些都與人類惡性腫瘤的形成有密切的關係。作為DNA複製解旋酶,MCM2-7本身的基因突變或異常表現也與許多人類疾病直接相關,例如MCM4基因突變可以導致乳腺癌。
鑒於MCM2-7複合物功能機制的重要性,過去三十年,相關領域研究人員對其進行大量的功能和結構方面的研究。由於其結構複雜,針對MCM2-7複合物的高分辨三維結構解析一直停滯不前,已成為其功能研究重要的限制因素。2013年下半年起,戴碧瓘研究團隊和高寧研究團隊攜手合作,利用清華大學冷凍電鏡平臺對MCM2-7複合物以及與相關功能因子結合的複合物進行結構解析。經過一年多的努力,課題獲得關鍵性的突破進展,解析出來自酵母菌的MCM2-7雙六聚體複合物接近原子分辨率(3.8 Å)的三維結構。
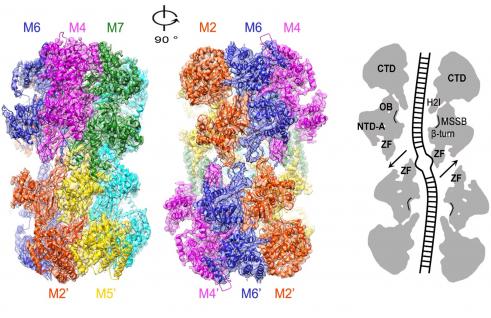
在這個結構中,兩個MCM2-7單六聚體疊加在一起,並相對於中心軸線有一定角度的傾斜和扭轉,在中心形成一個扭曲的中央通道。中央通道的大小正好匹配雙螺旋DNA的直徑。這些結構分析表明MCM2-7複合物直接參與複製起始時DNA最初的解鏈過程。這高分辨率的結構為高等生物的雙鏈DNA解旋酶複合物的組裝、激活和調控研究提供一個全新的框架。
香港科技大學生命科學部的翟元梁研究助理教授和清華大學生命學院李寧寧博士為該論文的共同第一作者。香港科技大學的戴碧瓘教授、翟元梁博士以及清華大學生命學院的高寧教授為通訊作者。該研究獲得了香港研究資助局(Research Grants Council of Hong Kong)、香港科技大學、國家科技部以及國家自然科學基金委員會的經費支持。
研究論文全文:http://www.nature.com/nature/journal/vaop/ncurrent/full/nature14685.html