2015年7月29日,香港科技大学戴碧瓘(Bik-Kwoon Tye)教授和清华大学的高宁教授的研究团队共同在《自然》(Nature)杂志以长文形式发表题为《真核生物DNA复制解旋酶MCM复合物的3.8 Å分辨率结构》(Structure of the Eukaryotic MCM Complex at 3.8 Å)的研究论文,首次揭示DNA复制解旋酶MCM2-7复合体的高分辨率(3.8 Å)冷冻电镜结构。这研究成果为人类认识及了解自身DNA复制起始过程的机制揭开新一页。
DNA是所有生物遗传信息的载体。六十多年前,当诺贝尔奖获得者Watson和Crick发现DNA双螺旋结构的时候,他们就预测到,在DNA复制过程中,需要解开紧密结合的双链DNA,以便互补的DNA双链各自作为范本进行复制。从那时起,关于DNA双螺旋解链机理的研究,一直是生物学领域的研究热点。
早在1983年,戴碧瓘教授在康奈尔大学的实验室,率先发现MCM2-7基因,并证明这些基因在真核生物DNA复制过程发挥非常重要的作用。随后的科学研究进一步发现,MCM2-7复合物负责在DNA复制起始和延伸阶段作为双链DNA的解螺旋酶。在真核生物细胞,整个DNA复制的过程都受到严格调控,以确保DNA遗传信息能被准确复制。复制过程中的异常或缺陷会导致基因组不稳定,包括DNA双链的断裂、基因突变、染色体缺失,这些都与人类恶性肿瘤的形成有密切的关系。作为DNA复制解旋酶,MCM2-7本身的基因突变或异常表现也与许多人类疾病直接相关,例如MCM4基因突变可以导致乳腺癌。
鉴于MCM2-7复合物功能机制的重要性,过去三十年,相关领域研究人员对其进行大量的功能和结构方面的研究。由于其结构复杂,针对MCM2-7复合物的高分辨三维结构解析一直停滞不前,已成为其功能研究重要的限制因素。2013年下半年起,戴碧瓘研究团队和高宁研究团队携手合作,利用清华大学冷冻电镜平台对MCM2-7复合物以及与相关功能因子结合的复合物进行结构解析。经过一年多的努力,课题获得关键性的突破进展,解析出来自酵母菌的MCM2-7双六聚体复合物接近原子分辨率(3.8 Å)的三维结构。
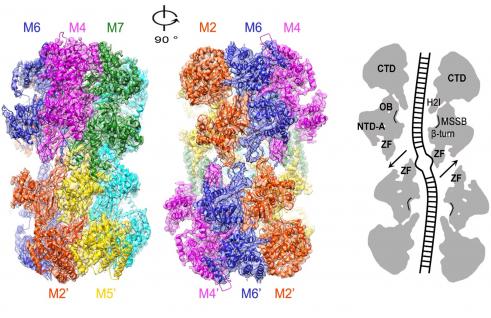
在这个结构中,两个MCM2-7单六聚体迭加在一起,并相对于中心轴线有一定角度的倾斜和扭转,在中心形成一个扭曲的中央通道。中央通道的大小正好匹配双螺旋DNA的直径。这些结构分析表明MCM2-7复合物直接参与复制起始时DNA最初的解链过程。这高分辨率的结构为高等生物的双链DNA解旋酶复合物的组装、激活和调控研究提供一个全新的框架。
香港科技大学生命科学部的翟元梁研究助理教授和清华大学生命学院李宁宁博士为该论文的共同第一作者。香港科技大学的戴碧瓘教授、翟元梁博士以及清华大学生命学院的高宁教授为通讯作者。该研究获得了香港研究资助局(Research Grants Council of Hong Kong)、香港科技大学、国家科技部以及国家自然科学基金委员会的经费支持。
研究论文全文:http://www.nature.com/nature/journal/vaop/ncurrent/full/nature14685.html